原创 JLT/CXB CBG资讯 2025年08月12日 13:51江苏
全文概述
最近,武汉理工大学木士春教授和李蓓副教授采用活化羟基诱导界面水质子交换策略加速了催化剂的碱性析氢反应(HER)动力学。Ru等金属表面大量活化羟基(OHad)的引不仅优化了金属活性位点的电子/能带结构和物理化学状态,而且OHad还积极地参与质子交换过程,优化了界面水分子的吸附和解离过程,从而加速HER动力学。该项研究证明了金属表面活化羟基对碱性析氢反应中界面水质子交换过程的调节作用,以及金属表面活化羟基-界面水质子交换策略的普适性。研究成果为高性能催化剂的设计提供了一种新的思路。武汉理工大学研究生蒋林涛和陈兴宝为论文的第一作者,李蓓副教授和木士春教授共同担任论文的通讯作者。相关研究成果发表于ACS Catal.(DOI: 10.1021/acscatal.4c07602)。
研究背景
多种中间体演变路径与电子-质子耦合转移过程显著影响催化反应效率。对于碱性析氢反应(HER),存在着界面水的吸附与解离和*H、*OH中间体的形成与脱附等复杂过程,严重减缓了HER反应动力学。因此,有必要改善碱性HER催化剂的中间体相互作用,以便更好地调节活性位点本征活性,降低反应能垒。然而,催化过程中将会受到因*H/*OH竞争性吸附导致的动力学阻碍,通过单一中间体行为调控不利于提升本征活性。OHad是一种电子有利的亲水质子受体,相较于纯的原子级金属活性中心更有利于与界面水物种相互作用,从而促进水吸附过程。另一方面,由于OHad直接参与反应形成额外的OH位点,避免了OH脱附步骤,加速了随后的水解离与*H脱附。可见,如果利用催化剂表面吸附的羟基物种(OHad)来直接参与HER过程,应有利于打破*H与*OH的竞争性吸附,从而显著提高电解水产氢效率。
本文亮点
1. 制备了一种具有核壳结构的Ru-Ni(OH)2预催化剂,并通过原位电化学活化进一步将预催化剂转化为同样具有核壳结构的R-Ru-Ni(OH)2催化剂,同时实现了Ru等金属表面活化OHad物种的引入。
2. 证明了金属表面活化OHad与界面水可发生显著的质子交换,实现了HER电子转移路径的优化,从而有效提升催化剂的HER本征活性。
图文解析

图1 (a) R-Ru-Ni(OH)2制备的示意图。(b, c) NF上Ru-Ni(OH)2和R-Ru-Ni(OH)2的SEM图像。(d, e) Ru-Ni(OH)2和R-Ru-Ni(OH)?的HRTEM图像。(f, g) 通过EDS映射得到的Ru-Ni(OH)2和R-Ru-Ni(OH)2相应的元素分布情况。(来源:ACS Catal. )
首先,分别通过水热和电化学活化等步骤构建核壳催化剂R-Ru-Ni(OH)2/NF(图1a-c)。其中,Ru核的直径为80-100 nm,Ni(OH)2壳层厚度大约为20 nm(图1d,e)。EDS表明Ru主要分布在Ru-Ni(OH)2纳米球内部,而Ni,O则分布在Ru-Ni(OH)2纳米球表面(图1f, g)。这些研究结果有力证明了Ru-Ni(OH)2核壳结构的形成。
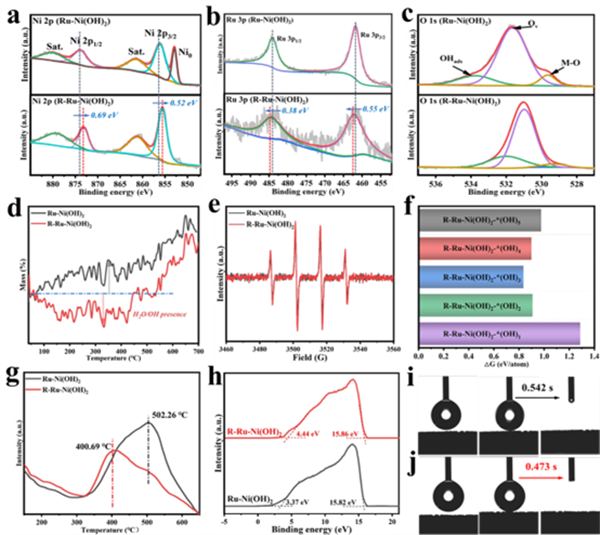
图2 (a, b, c) R-Ru-Ni(OH)2和Ru-Ni(OH)2的Ni 2p、Ru 3p和O 2p的高分辨率XPS。(d) R-Ru-Ni(OH)2和Ru-Ni(OH)2在氩气氛围下的TG曲线。(e) R-Ru-Ni(OH)2和Ru-Ni(OH)2的EPR谱图。(f) 不同数量OH吸附基团的R-Ru-Ni(OH)2-*(OH)x的形成能。(g) R-Ru-Ni(OH)2和Ru-Ni(OH)2的H2-TPD曲线。(h) R-Ru-Ni(OH)2和Ru-Ni(OH)2的UPS谱图。(i) Ru-Ni(OH)2和 (j) R-Ru-Ni(OH)2的水接触角测试。(来源:ACS Catal. )
XPS、TG、EPR等测试证明了R-Ru-Ni(OH)2催化剂Ru表面羟基基团的成功引入(图2a-e)。进一步结合DFT计算验证了OHad更容易吸附在Ru表面(图2f)。H2-TPD、UPS及水接触角等测试验证了金属表面活化羟基基团的存在对于氢脱附过程、能带结构和亲水性的改善作用(图2g-i)。这些研究共同证明了R-Ru-Ni(OH)2催化剂表面确实存在着丰富的亲水羟基基团。
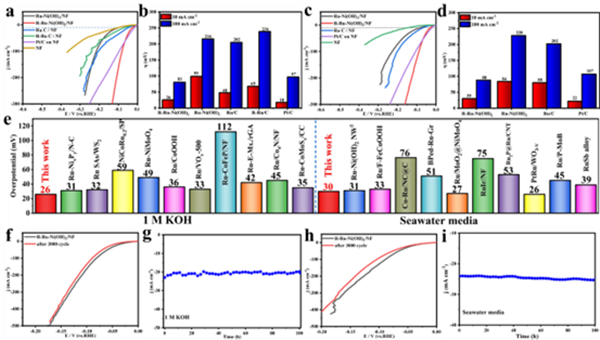
图3 催化剂在 (a, b) 1 M KOH溶液和 (c, d) 海水介质中的LSV曲线及相应过电位(@10和100 mA cm-2)。(e) 在碱性介质中,R-Ru-Ni(OH2与近期报道的钌基电催化剂在10 mA cm-2时析氢反应(HER)性能的比较。R-Ru-Ni(OH)2在 (f, g) 1 M KOH溶液和 (h, i) 海水介质中的3000次循环伏安稳定性和电流密度随时间变化的曲线。(来源:ACS Catal. )
在所有催化剂中,R-Ru-Ni(OH)2催化剂表现出最佳的活性。在电流密度为10与100 mA cm-2条件下,该催化剂的过电位分别为26与81 mV,可与商业Pt/C性能(18,97 mV)相媲美(图3a-e)。此外,当催化剂的CV循环达到3000圈,i-t运行长达100 h时,催化剂仍能保持高的稳定性,证明R-Ru-Ni(OH)2亦具有优异的电化学稳定性(图3f-i)。同时,对于Ru-M(OH)2/MF(M = Fe、NiFe、Cu)和M-Ni(OH)2/NF(M = Ir、Pt),经电化学活化后其碱性HER性能普遍得到改善。证明羟基-界面水质子交换策略具有通用性。

图4 (a) Ru-Ni(OH)2和 (b) R-Ru-Ni(OH)2在1 M KOH溶液中从0.024至-0.426 V vs.RHE的原位拉曼光谱。(c, e) Ru - Ni(OH)2和 (d, f) R-Ru-Ni(OH)2在从0.024至-0.676 V vs.RHE的原位衰减全反射表面增强红外吸收光谱(ATR-FTIR)。(g) R-Ru-Ni(OH)2和Ru-Ni(OH)2的动力学同位素效应(KIE)值。(h) R-Ru-Ni(OH)2在1 M KOD/D2O溶液中经CV活化后,通过原位微分电化学质谱(DEMS)检测的产氢信号。(i) 氘标记的R-Ru-Ni(OH)2的DEMS测试示意图。(来源:ACS Catal. )
原位拉曼/红外光谱(图4a-f)测试结果证明,R-Ru-Ni(OH)2拥有更多的表面羟基参与反应,改善了OH中间体演变动力学,有利于界面水的质子交换过程。R-Ru-Ni(OH)2计算的KIE值更低(图4g),表明HER中O-H更容易断裂以及水解离的加速。DEMS测试结果表明,在含氘(D)的电解液标记之后,R-Ru-Ni(OH)2出现了明显的HD信号,证明了质子交换过程的存在。这些研究结果有力地证明了稳定的表面活化羟基能够显著参与OH-H2O质子交换反应,促进HER动力学(图4h,i)。
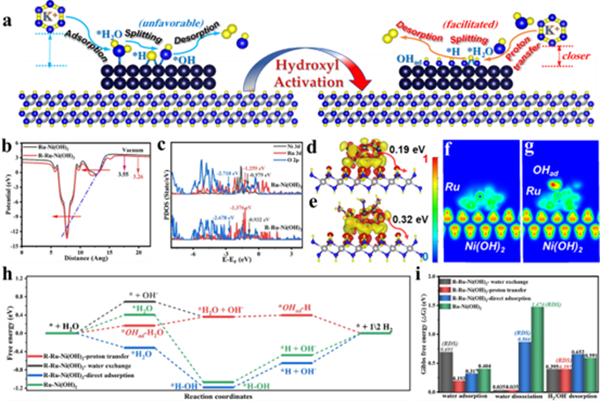
图5 (a) Ru-Ni(OH)2在HER过程中活化前后电子转移及反应中间体演变路径的示意图。(b) R-Ru-Ni(OH)2和Ru-Ni(OH)2的功函数。(c) R-Ru-Ni(OH)2和Ru-Ni(OH)2中Ru、Ni、O原子的部分态密度(PDOS)。(d) Ru-Ni(OH)2和 (e) R-Ru-Ni(OH)2的Bader电荷(DCD)。(f) Ru-Ni(OH)2和 (g) R-Ru-Ni(OH)2的电子局域函数(ELF)。 (h) R-Ru-Ni(OH)2以及Ru-Ni(OH)2中Ru位点在不同路径下的HER反应的吉布斯自由能变化 (i) R-Ru-Ni(OH)2和Ru-Ni(OH)2中Ru位点在不同路径下的水吸附、水解离和氢/羟基解吸的能垒。(来源:ACS Catal. )
最后,作者借助DFT计算,进一步证明Ru-Ni(OH)2核壳催化剂羟基活化后HER过程中电子结构与中间体演变路径的改善(图5a)。以Ru-OHad为反应位点,可实现更低能垒的质子交换过程,从而促进液态水转移到催化剂表面;同时,在羟基位点存在的条件下加速水解离与*H脱附进程。通过WF、PDOS、DCD、ELF以及吉布斯自由能计算,证明了活化OHad位点的电子局域化与能带改善(图5b-i)。表面活化的OHad位点直接参与并优化了OH-H2O质子交换反应,实现了水吸附解过程的加速。同时,由于额外OHad位点的存在降低了*H脱附能垒,极大地提高了催化剂的反应活性。
总之,作者通过电化学活化策略成功地将羟基物种引入到Ru-Ni(OH)2核壳催化剂的Ru表面,并验证了活化羟基物种能直接促进碱性HER反应。原位光谱/质谱结合DFT计算有力验证了OHad位点的存在一方面能够与界面水发生具有更低能垒的质子交换,加速水吸附-解离步骤过程,另一方面又能降低*H脱附能垒,从而双向优化了析氢反应动力学。此外,该电化学激活策略亦表现出通用性。